 La empresa Biotrial, portuguesa, patrocinaba en el Hospital Universitario de Rennes (Francia), un ensayo clínico en Fase I sobre un analgésico oral destinado a pacientes con dolor crónico. El resultado en los seis primeros voluntarios, de entre los 90 inscritos inicialmente, no ha podido ser peor: cinco de ellos con graves problemas neurológicos -que podrían derivar en discapacidades permanentes- y un sexto, varón de 49 años, fallecido.
La empresa Biotrial, portuguesa, patrocinaba en el Hospital Universitario de Rennes (Francia), un ensayo clínico en Fase I sobre un analgésico oral destinado a pacientes con dolor crónico. El resultado en los seis primeros voluntarios, de entre los 90 inscritos inicialmente, no ha podido ser peor: cinco de ellos con graves problemas neurológicos -que podrían derivar en discapacidades permanentes- y un sexto, varón de 49 años, fallecido.
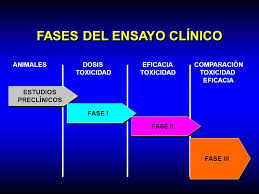
Ignoro si a día de hoy existe alguna explicación plausible sobre lo sucedido, y convendrá seguir al detalle la evaluación de unos hechos que pueden tildarse de excepcionales, toda vez que los ensayos con nuevos fármacos están sujetos a una estricta regulación y con normativa que, de seguirse en su integridad como es la regla, hace prácticamente imposible semejante desenlace. Para que un medicamento novedoso pueda ser administrado a voluntarios (sanos o afectos de la patología que se pretende mejorar), debe haber superado con éxito los oportunos estudios preclínicos -de laboratorio, con animales…-. Sólo tras estos requisitos podrá administrarse a humanos y en distintas fases perfectamente establecidas: de la Fase I, cual ha sido el caso (evaluación de seguridad y tolerancia) a la Fase IV.
 Por lo que concierne a nuestro país, este mismo mes ha entrado en vigor (mera coincidencia en el tiempo y nada que ver con lo sucedido) el Real Decreto 1090/2015, que aporta algunas modificaciones respecto al vigente hasta aquí, de 2004. A vuelapluma y con el fin de que los no iniciados en este ámbito cobren conciencia de las garantías que se exigen en la investigación clínica, convendrá subrayar que cualquier producto ha de ser evaluado previamente por la Agencia Española del Medicamento y un Comité Ético de Investigación Clínica debidamente acreditado, antes de que se autorice su uso en ensayos estrictamente controlados. Asimismo, tanto los investigadores como los centros e instalaciones deben probar su idoneidad frente a las instancias pertinentes (Registro Español de Estudios Clínicos), una vez que los protocolos y ficha técnica del preparado hayan sido aprobados.
Por lo que concierne a nuestro país, este mismo mes ha entrado en vigor (mera coincidencia en el tiempo y nada que ver con lo sucedido) el Real Decreto 1090/2015, que aporta algunas modificaciones respecto al vigente hasta aquí, de 2004. A vuelapluma y con el fin de que los no iniciados en este ámbito cobren conciencia de las garantías que se exigen en la investigación clínica, convendrá subrayar que cualquier producto ha de ser evaluado previamente por la Agencia Española del Medicamento y un Comité Ético de Investigación Clínica debidamente acreditado, antes de que se autorice su uso en ensayos estrictamente controlados. Asimismo, tanto los investigadores como los centros e instalaciones deben probar su idoneidad frente a las instancias pertinentes (Registro Español de Estudios Clínicos), una vez que los protocolos y ficha técnica del preparado hayan sido aprobados.  Con tales requisitos, extensivos a los países desarrollados, lo ocurrido en Rennes constituye una excepción que exigirá de meticuloso análisis para aclarar esa fatal equivocación. ¿Hubo algún defecto en la evaluación preclínica? ¿Error humano respecto a la dosis suministrada? Sea como fuere, tanto la población general como los profesionales de la sanidad esperamos una información exhaustiva que termine con las dudas. En bien de todos.
Con tales requisitos, extensivos a los países desarrollados, lo ocurrido en Rennes constituye una excepción que exigirá de meticuloso análisis para aclarar esa fatal equivocación. ¿Hubo algún defecto en la evaluación preclínica? ¿Error humano respecto a la dosis suministrada? Sea como fuere, tanto la población general como los profesionales de la sanidad esperamos una información exhaustiva que termine con las dudas. En bien de todos.

Conviene subrayar que la primera Fase I implica el uso de un medicamento que NUNCA se ha usado en seres humanos con anterioridad. Del medicamento se sabe un porrón en ratones, perros y hasta chimpancés, pero resulta que las personas ostentan ciertas diferencias. (Por ejemplo, se quejan más.)
Es cierto que se trata de algo excepcional, pero conviene recordar un episodiosemejante, hace muchos años, precisamente con uno de los quimioterápicos más corrientes hoy día: el cisplatino. Empezóse a utilizar en seres humanos e inesperadamente, con dosis ínfimas, se registraron muertes por fracaso renal. ¿El intríngulis? Que el riñón de los roedores es resistente al cisplatino, y en ellos no surge la insuficiencia renal tan pronto.
La cosa tuvo a medio plazo cierto remedio (y quizá suceda así con el medicamento portugués), pero esto me hace reflexionar sobre un punto crucial. Los ensayos de Fase I en ONCOLOGÍA se llevan a cabo necesariamente en ENFERMOS, justo porque cabe esperar «alguna» toxicidad. En cambio, otras ramas de la Medicina aceptan a «voluntarios sanos». Pues bien: quizá sea hora de rechazar esa figura. Quizá sea oportuno que todo medicamento «novedoso» se pruebe en un contexto clínico, es decir en gente con ALGÚN problema de salud, a cuya mitigación pueda contribuir la novedad farmacéutica. Que no se cobre por tentar a la suerte, vaya, sino que la Medicina sirva a fines menos crematísticos.
Obviamente, eso enlentecerá la investigación, pero ya tengo dicho por ahí que la enfemedad de nuestro tiempo es la prisa. Tenemos prisa por llegar a no sabemos dónde, con el riesgo de no percatarnos de que hemos llegado al lugar exacto o, peor aún, de comprobar demasiado tarde que hemos llegado demasiado pronto.
Me gustaMe gusta
Sí, recuerdo los problemas con el Platino. Y respecto a los ensayos sólo con enfermos, también creo que te asiste buena parte de razón. En cualquier caso, estoy intrigado por saber qué es lo que ha sucedido en Francia. Entre otras cosas, me pregunto por qué una compañía portuguesa inició la fase clínica allí.
Me gustaMe gusta
Por partes.
Los preclínicos con animales son necesarios, la clave es el cuidado extremo que ha de tenerse en el paso a la Fase I en humanos. Contemplar TODAS las diferencias que podemos tener el ratón, o el animal en cuestión, en el recorrido por el organismo del medicamento, desde su administración hasta su eliminación.
Es de sospechar que los receptores de los lugares de acción de los medicamentos sean diferentes entre humanos y animales (si ya lo son entre humanos y humanos) Y esto hablando solo del mecanismo de acción, amén de que la persona pueda comunicar, sentir más, y muchos más aspectos… (¿estará ahí la razón del problema?)
También defiendo los ensayos con enfermos, pues realizarlos con sanos introduce sesgos. Y es posible que no se enlentezca tanto el proceso (a no ser que se trate de enfermedades raras)
Y por último, echo en falta más información sobre este hecho. Creo que la están silenciando. Y es necesario que sepamos con exactitud qué ha ocurrido.
Pienso que a partir de ahora me fijaré más en qué animales se ha hecho el preclínico y me preguntaré porqué.
Me gustaMe gusta
Es posible que a la Industria promotora no le interese que salga todo a la luz… Hay que seguir el tema.
Me gustaMe gusta
Como muy lega en estas lides, pero si la ley española es más intransigente con los nuevos sesgos, ¿ que sucede cuando llega un medicamento testado en Estados Unidos, sin ninguna contraindicación alli? ¿ se dá el medicamento por bueno, o bien se realizan aquí otras pruebas para reconfirmarlo?.
Sé por ejenplo, que hay medicamentos que en Canadá están a la venta pero en EEUU no y a la inversa. ¿ Cual es el motivo? ¿realizan sus propios ensayos clínicos y los retirán? ¿ hacemos nosotros lo mismo?
Me gustaMe gusta
No es más intransigente; los países desarrollados (de otros lo ignoro) tienen todos normas para los ensayos clínicos muy similares; además, muchos de ellos se realizan en centros de varios países a la vez (multinacionales). Cosa distinta es que, tras los ensayos con éxito, el medicamento pueda prescribirse en algunos países y no en otros; ahí entran en consideración otras cuestiones, sobre todo económicas (precio del fármaco, aceptación del costo por parte del sistema público de salud…).
Me gustaMe gusta
Gracias!
Me gustaMe gusta